Einführung:
Akuter Husten ist eines der in Arztpraxen am häufigsten festgestellten Symptome, denen meist ein viraler Infekt der unteren Atemwege zugrunde liegt. Zubereitungen aus Efeublättern sind in der Behandlung dieser Symptome seit langem etabliert und ihre Wirkweise ist zunehmend detailliert untersucht. Der Efeublätter-Trockenextrakt EA 575 (DEV 5-7,5:1, Auszugsmittel: 30% Ethanol) ist besonders gut untersucht und in dieser randomisierten, placebokontrollierten und multizentrischen klinischen Prüfung zur Behandlung von 181 erwachsenen Patienten mit akutem Husten eingesetzt.
Patienten und Methodik:
An dieser Studie nahmen 181 erwachsene Patienten im Alter von 18-75 Jahren mit der Diagnose „akuter Husten“ Teil. Einschlusskriterien stellten eine eingangs festgestellte Hustenschwere von ≥ 50 mm auf der Visuellen Analogskala (VAS), ein Bronchitis Severity Score (BSS) von ≥ 10 und ein Visual Category Descriptive (VCD) Wert von ≥ 2 dar. Die Symptome sollten seit 2-3 Tagen vor Behandlungsbeginn aufgetreten sein.
Die wichtigsten Ausschlusskriterien waren allergisches Asthma bronchiale, chronische oder vererbte Lungenerkrankungen, eine Anamnese von chronischer Gastritis oder Magengeschwüre. Ausgeschlossen wurde auch die gleichzeitige Behandlung mit Corticoiden, β2-Sympathomimetika, anderen Expektorantien, Antitussiva, Acetylsalicylsäure, NSAID, Antibiotika, Antihistaminika oder ACE-Hemmer 7 Tage vor Behandlungsbeginn. Auch Schwangere, Stillende, sowie Patienten mit Fieber (Körpertemperatur > 38,3 °C) wurden nicht eingeschlossen.
Dem Prüfplan entsprechend erhielten die Patienten entweder 3 Mal täglich 5 mL des Prüfpräparates (entsprechend einer Tagesdosis von 105 mg) oder Placebo. Der Behandlungszeitraum betrug eine Woche mit einer Abschlussvisite 14 Tage nach Behandlungsbeginn.
Der primäre Endpunkt bestand in der Änderung der Hustenschwere gemessen über VAS von Therapiebeginn bis zum Behandlungsende (Tag 7). Sekundäre Endpunkte bestanden unter anderem in der Änderung des BSS und des VCD Werts.
Ergebnisse:
Die Hustenschwere (gemessen über VAS) der mit Verum behandelten Patienten verbesserte sich über die gesamte Therapiedauer im Vergleich zur Placebo-Gruppe signifikant (AUC0-168 h, p < 0,0001). Bereits innerhalb von 48 h ist eine statistisch signifikante Reduktion der Hustenschwere und nach 7 Tagen eine deutliche Überlegenheit gegenüber Placebo zu beobachten (Abb. 1).
Die durch VCD Score erhobene Hustenschwere der mit Verum behandelten Gruppe reduzierte sich ebenfalls über die gesamte Therapiedauer im Vergleich zur Placebo-Gruppe signifikant zum Therapieende um 60%.
Der durch den Arzt in Zusammenarbeit mit dem Patienten erfasste Bronchitis-Summenscore (BSS) reduzierte sich in der mit EA 575 behandelten Gruppe im Vergleich zur Placebo-Gruppe bereits innerhalb von 48 h signifikant (Abb. 2).
Die mit Verum behandelte Gruppe zeigte selbst 7 Tage nach Therapieende noch einen signifikanten Vorteil bezüglich der Linderung der Hustenschwere im Vergleich zur Placebo-Gruppe.
Sehr gute Verträglichkeit: Es zeigten sich keine therapiebezogenen, unerwünschten Ereignisse.
Fazit:
Die gute Wirksamkeit und Verträglichkeit von Efeublätter-Trockenextrakt EA 575 bei erwachsenen Patienten konnte innerhalb dieser Studie belegt werden. Die mit EA 575 behandelten Patienten zeigten in allen geprüften Parametern eine klare Überlegenheit gegenüber Placebo, welche bereits innerhalb von 48 h sichtbar war.
Abbildungen:
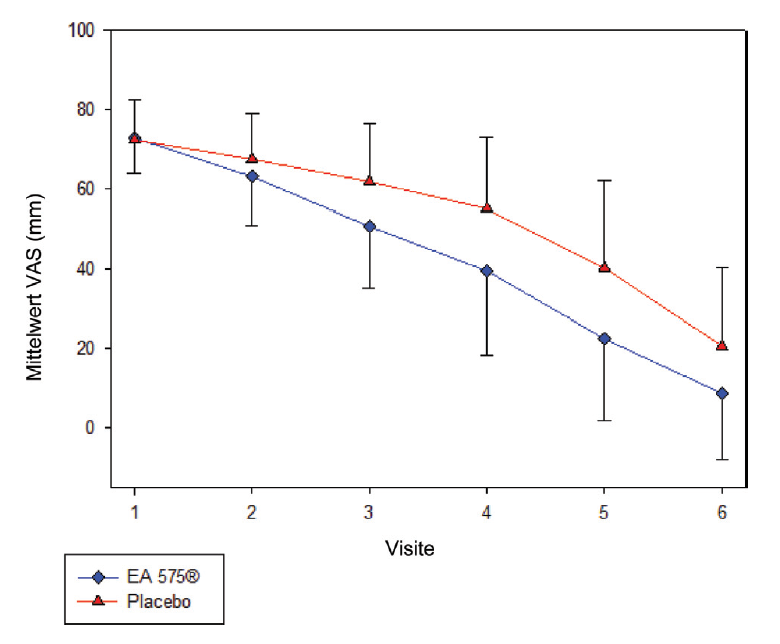
Abb. 1: Husten-Schweregrad auf der Visuellen Analogskala (VAS) (Mittelwert + SD) über die Zeit
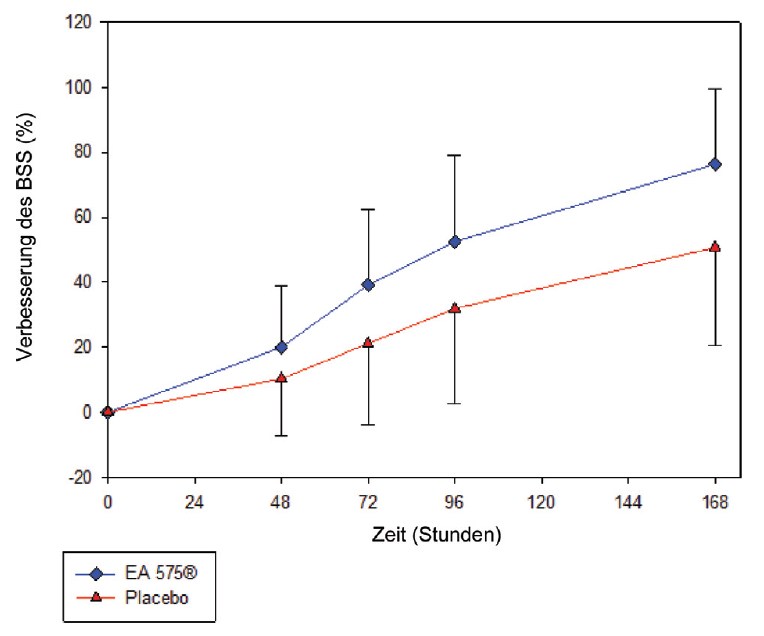
Abb. 2: Relative Verbesserung des BSS gegenüber dem Baseline-Wert
(Quelle: Schaefer, A., et al. (2016). "A randomized, controlled, double-blind, multi-center trial to evaluate the efficacy and safety of a liquid containing ivy leaves dry extract (EA 575) vs. placebo in the treatment of adults with acute cough.")