Einführung:
Trotz der internationalen Häufigkeit der Diagnose der akuten Bronchitis findet eine Behandlung oftmals nicht evidenzbasiert oder leitliniengerecht statt. Auch in Anbetracht der Tatsache, dass trotz besseren Wissens eine antibiotische Therapie vielerorts voreilig durchgeführt wird, ist es wichtig wirksame Alternativen zur Behandlung der akuten Bronchitis zu erforschen und zu etablieren. Zu diesem Zwecke führten Schaefer et al. eine randomisierte, placebokontrollierte multizentrische klinische Prüfungen in fünf Arztpraxen mit dem Efeublätter-Trockenextrakt EA 575 in zwei verschiedenen Dosierungsschemata während der Erkältungssaison 2016/17 an 209 erwachsenen Patienten durch.
Patienten und Methodik:
An dieser Studie nahmen 209 erwachsene Patienten im Alter von 18-73 Jahren mit der Diagnose „akute Bronchitis“ teil. Einschlusskriterien stellten eine eingangs festgestellte Hustenschwere von ≥ 50 mm auf einer Visuellen Analogskala (VAS), ein Bronchitis Severity Score (BSS) von ≥ 10 und ein Visual Category Descriptive (VCD) Wert von ≥ 2 dar. Die Symptome sollten seit 2-3 Tagen vor Behandlungsbeginn aufgetreten sein.
Die wichtigsten Ausschlusskriterien waren allergisches Asthma bronchiale, chronische oder vererbte Lungenerkrankungen, eine Anamnese von chronischer Gastritis oder Magengeschwüre. Ausgeschlossen wurde auch die gleichzeitige Behandlung mit Corticoiden, β2-Sympathomimetika, anderen Expektorantien, Antitussiva, Acetylsalicylsäure, NSAID, Antibiotika, Antihistaminika oder ACE-Hemmer 7 Tage vor Behandlungsbeginn. Auch Schwangere, Stillende, sowie Patienten mit Fieber (Körpertemperatur > 38,3 °C) wurden nicht eingeschlossen.
Das Patientenkollektiv wurde entsprechend dem Prüfplan im Verhältnis 2:2:1:1 in zwei Verum-Gruppen und zwei Placebo-Gruppen aufgeteilt, um ein neues Dosierungsschema gegenüber dem gültigem zu vergleichen. Die Patienten erhielten entweder 3 Mal täglich 5 mL bzw. 2 Mal täglich 7,5 mL des Prüfpräparates (entsprechend einer Tagesdosis von 105 mg) oder Placebo. Der Behandlungszeitraum betrug eine Woche mit einer Abschlussvisite 14 Tage nach Behandlungsbeginn.
Der primäre Endpunkt bestand in der Änderung der Symptomschwere gemessen über BSS von Therapiebeginn bis zum Behandlungsende (Tag 7). Sekundäre Endpunkte bestanden unter anderem in der Änderung des VAS und des VCD Werts.
Ergebnisse:
Der durch den Arzt in Zusammenarbeit mit dem Patienten erfasste Bronchitis-Summenscore (BSS) reduzierte sich in der mit Efeublätter-Trockenextrakt EA 575 behandelten Gruppe im Vergleich zur Placebo-Gruppe innerhalb von 72 h signifikant und nach 7 Tagen war eine deutliche Überlegenheit gegenüber Placebo zu beobachten. Hierbei konnte zu keinem Messzeitpunkt ein statistisch signifikanter Unterschied zwischen den beiden Dosierungsschemata gefunden werden (Abb. 1).
Die durch VCD Score erhobene Hustenschwere der mit Verum behandelten Gruppe reduzierte sich ebenfalls über die gesamte Therapiedauer im Vergleich zur Placebo-Gruppe signifikant zum Therapieende (Abb. 2).
Die mit Verum behandelte Gruppe zeigte selbst 7 Tage nach Therapieende noch einen signifikanten Vorteil bezüglich der Linderung der Hustenschwere im Vergleich zur Placebo-Gruppe (Abb. 1 und 2).
Die Hustenschwere (gemessen über VAS) der mit Verum behandelten Patienten verbesserte sich über die gesamte Therapiedauer im Vergleich zur Placebo-Gruppe signifikant (AUC0-168 h, p < 0,0001). Innerhalb von 72 h ist eine statistisch signifikante Reduktion der Hustenschwere und nach 7 Tagen eine deutliche Überlegenheit gegenüber Placebo zu beobachten.
Sehr gute Verträglichkeit: Es zeigten sich nur ein therapiebezogenes, unerwünschtes Ereignis.
Fazit:
Die Ergebnisse der ersten kontrollierten klinischen Prüfung (Schaefer et al. 2016) konnten bestätigt werden. Die gute Wirksamkeit und Verträglichkeit von Efeublätter-Trockenextrakt EA 575 bei erwachsenen Patienten konnte innerhalb dieser Studie zusätzlich auch für ein neues Dosierungsschema von 2 Mal 7,5 mL pro Tag belegt werden. Die mit EA 575 behandelten Patienten zeigten auch 7 Tage nach Therapieende in allen geprüften Parametern eine Überlegenheit gegenüber Placebo.
Abbildungen:
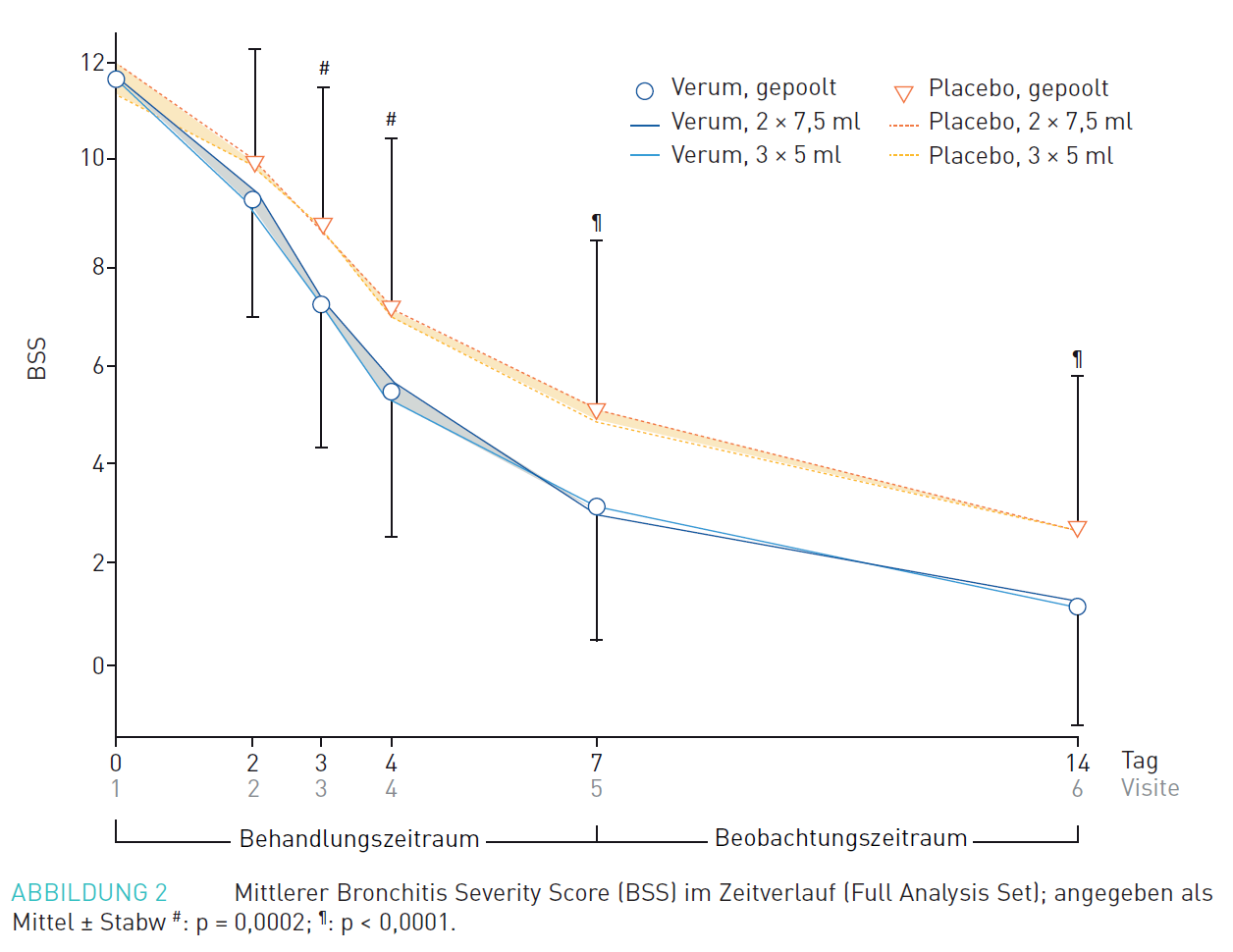
Abb. 1: Mittlerer Bronchitis Severity Score (BSS) im Zeitverlauf; angegeben als Mittel ± Standardabweichung #: p = 0,0002; ¶: = p < 0,0001
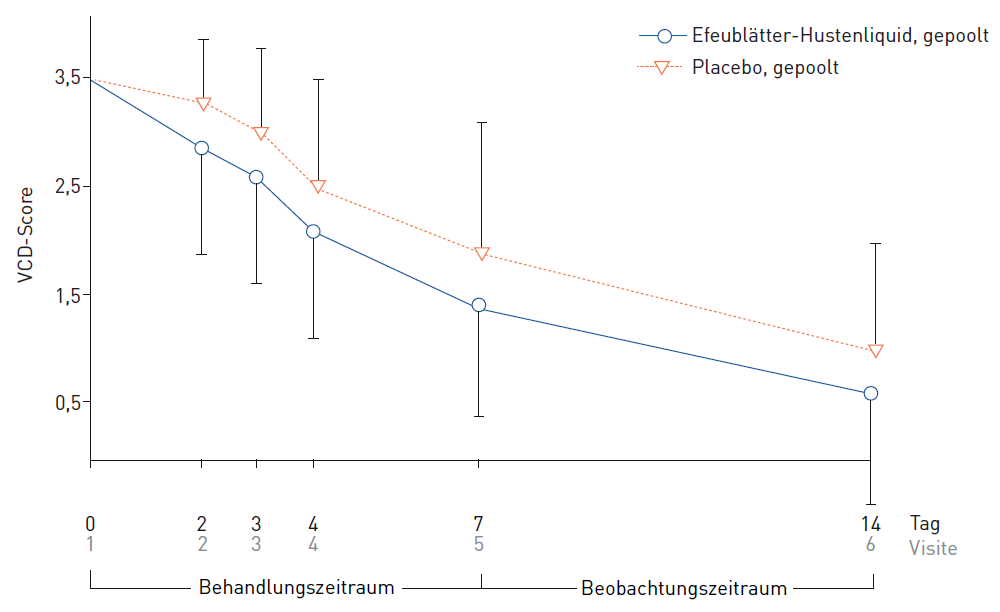
Abb. 2: Entwicklung des VCD-Scores (Verbal Category Descriptive) der gepoolten Verum- und Placebogruppen von Visite V1 bis V6; angegeben als Mittel ± Standardabweichung